Química (palabra que podría provenir de los términos griegos χημία o χημεία, quemia y quemeia respectivamente)[1] es la ciencia que estudia tanto la composición, estructura y propiedades de la materia como los cambios que ésta experimenta durante las reacciones químicas y su relación con la energía.[2] Es definida, en tanto, por Linus Pauling, como la ciencia que estudia las sustancias, su estructura (tipos y formas de acomodo de los átomos), sus propiedades y las reacciones que las transforman en otras sustancias.[3]
La química moderna se fue formulando a partir de la alquimia, una práctica protocientífica de carácter filosófico, que combina elementos de la química, la metalurgia, la física, la medicina, la biología, entre otras ciencias y artes. Esta fase termina al ocurrir la llamada, Revolución de la química, basada en la ley de conservación de la masa y la teoría de la oxígeno-combustión postuladas por el científico francés, Antoine Lavoisier.[4]
Las disciplinas de la química se agrupan según la clase de materia bajo estudio o el tipo de estudio realizado. Entre éstas se tienen la química inorgánica, que estudia la materia inorgánica; la química orgánica, que estudia la materia orgánica; la bioquímica, que estudia las substancias existentes en organismos biológicos; la fisicoquímica, que comprende los aspectos energéticos de sistemas químicos a escalas macroscópicas, moleculares y atómicas, o la química analítica, que analiza muestras de materia y trata de entender su composición y estructura.[5]
quimica
jueves, 26 de febrero de 2015
los estados quimicos
Los estados de agregación y la teoría cinética
Partículas en continuo movimiento
Todo en el Universo está formado por materia. La materia se puede encontrar en 3 estados de agregación o estados físicos: sólido, líquido y gaseoso. Sus propiedades son:
| SÓLIDO | LÍQUIDO | GAS |
 |  |  |
|
|
|
Puedes ver más información en esta página web.
La teoría cinética
La teoría cinética nos indica que la materia, sea cual sea su estado, está formada por partículas tan diminutas que no se pueden observar a simple vista y que, además, se encuentran en continuo movimiento. Ese estado de movimiento depende de la temperatura, siendo mayor conforme más alto es el valor de dicha temperatura.
Para comprender mejor la teoría cinética puedes trabajar con esta webquest.
Realiza las siguientes actividades.
Los estados de agregación y la teoría cinética
La teoría cinética es capaz de explicar porqué una misma sustancia se puede encontrar en los 3 estados: sólido, líquido y gas. Esto depende sólo de la manera de agruparse y ordenarse las partículas en cada estado.
Estado sólido: La teoría cinética explica este estado como puede verse en esta página web y en esta otra.
Estado líquido: La teoría cinética explica este estado en esta página web y en esta otra.
Estado gaseoso: La teoría cinética lo explica como puede verse aquí y en esta otra página.
La temperatura de los cuerpos y la teoría cinética
Cuando calentamos un cuerpo, sus partículas se mueven más deprisa con lo cual aumentan su energía cinética. Si lo enfriamos ocurre lo contrario: disminuye la energía cinética de las partículas. La energía cinética es la energía que tiene un cuerpo en movimiento.
La temperatura es la medida de la energía térmica (energía cinética media de todas las partículas que forman un cuerpo) de una sustancia. Se mide con un termómetro. Las escalas más empleadas para medir esta magnitud son la Escala Celsius (o centígrada) y la Escala Kelvin. 1ºC es lo mismo que 1 K, la única diferencia es que el 0 en la escala Kelvin está a - 273 ºC.
En la escala Celsius se asigna el valor 0 (0 ºC) a la temperatura de congelación del agua y el valor 100 (100 ºC) a la temperatura de ebullición del agua. El intervalo entre estas dos temperaturas se divide en 100 partes iguales, cada una de las cuales corresponde a 1 grado.
En la escala Kelvin se asignó el 0 a aquella temperatura a la cual las partículas no se mueven (temperatura más baja posible). Esta temperatura equivale a -273 ºC de la escala Celsius.
Para convertir ambas temperaturas, tenemos que tener en cuenta que:
T (K) = t(ºC) + 273
formulas quimicas
a. Conceptos de símbolo y fórmula.
Símbolo químico. Es la representación escrita y abreviada del nombre de un elemento químico.
Todos los elementos químicos tienen su propio nombre, el cual se ha - abreviado mediante un símbolo que está compuesto o formado por una, dos y hasta tres letras; por ejemplo, hay un elemento químico llamado Calcio cuyo nombre se ha abreviado a dos letras Ca, que forman así el símbolo del Calcio; así pues, se establece simplemente que los símbolos químicos representan a los elementos o sustancias simples.
Formula química. Es la representación escrita y abreviada de una sustancia.
Las formulas son como una clave química o una notación (representación por medio de signos convencionales). Cada tipo de sustancia existente tiene su propia formula, o sea, una formula sirve para identificar a una sustancia en particular.
b. Tipos de fórmulas.
Existen tres tipos fundamentales o principales de fórmulas: molecular, desarrollada o estructural y semi-desarrollada.
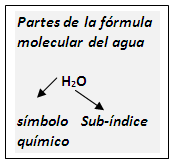
Formula molecular: es la representación gráfica y real de una sustancia. Es conocida también como fórmula condensada. Esta fórmula nos indica que clase de elementos químicos componen a la sustancia que representa (aspecto cualitativo), así como la cantidad de átomos de cada elemento (aspecto cuantitativo); la misma está compuesta de Símbolos químicos y números. Los números son enteros y pequeños, llamados subíndices, e indican la cantidad de átomos del elemento químico que lo conlleva; se ubican en la parte inferior derecha de cada símbolo, y cuando no aparece ningún número como sub-índice entonces se supone que es uno (1), el cual nunca se escribe. Observe las situaciones siguientes:
H2 es la fórmula de dos átomos de Hidrogeno unidos (molécula).
O es el símbolo químico de un átomo de Oxigeno; no es una formula.
O2 es la fórmula molecular del Oxigeno (sustancia simple).
H2O es la fórmula de una molécula de agua (sustancia compuesta).
Más ejemplos de formula molecular.
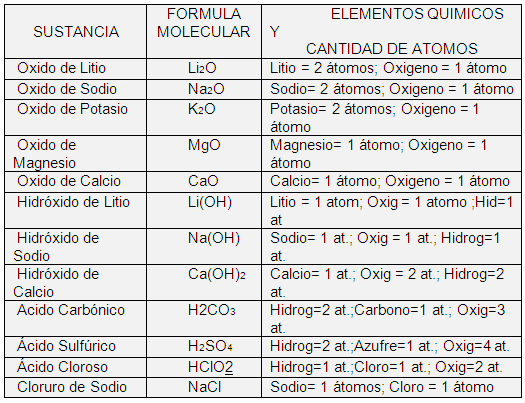
Observe que todas las formulas anteriores tienen coeficiente uno (1), por lo que cada una de ellas representa tan solo a una molécula de su respectiva sustancia. De aquí proviene su nombre de formula molecular.
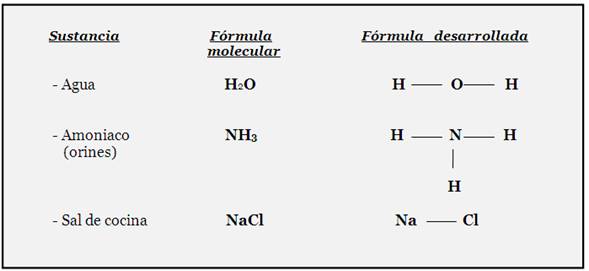
Formula desarrollada: es la representación espacial de una molécula de cualquier sustancia, mediante todos sus símbolos y enlaces químicos (guiones).
También se conoce como fórmula estructural. Los símbolos químicos se unen mediante guiones o líneas de Lang- muir, las que representan a los enlaces químicos, formándose así toda una estructura.
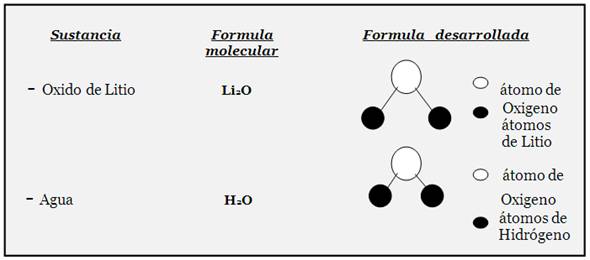
Otra manera de representar a la formula desarrollada o estructural es la siguiente:
materiales de calentamiento
Mechero de alcohol
Un encendedor, también llamado mechero o yesquero, es un dispositivo pirotécnico portátil usado para generar una llama.
Mechero de bunsen

Es un utensilio metálico que permite calentar sustancias. Este mechero de gas que debe su nombre al químico alemán ROBERT W. BUNSEN. Puede proporciona una llama caliente (de hasta 1500 grados centígrados), constante y sin humo, por lo que se utiliza mucho en los laboratorios. Está formado por un tubo vertical metálico, con una base, cerca de la cual tiene la entrada de gas, el tubo también presenta un orificio para la entrada de aire que se regula mediante un anillo que gira. Al encender el mechero hay que mantener la entrada del aire cerrada; después se va abriendo poco a poco. Para apagar el mechero se cierra el gas. Con ayuda del collarín se regula la entrada de aire. Para lograr calentamientos adecuados hay que regular la flama del mechero a modo tal que ésta se observe bien oxigenada (flama azul).
Hornilla Electrica

Aquel en que se produce calor por medio de la energía eléctrica. Puede ser de resistencia, de arco y de inducción.Horno manual de barro refractario o metal, que toma gralte. el nombre del combustible que se consume
Cápsula de porcelana

Al usar la capsula de porcelana se debe tener en cuenta que esta no puede estar vencida, pues de lo contrario, podría llegar a estallar.
Crisoles

Rejilla

Sirve para filtrar
Pinzas para crisol
Permiten sujetar crisoles
Pinza de madera

Una pinza o pinzas es una herramienta cuyos extremos se aproximan para sujetar algo. Funciona con el mecanismo de palancas simples
instrumentos quimicos
Tubos de ensayo

Gradilla
Refrigerante de rosario
Refrigerante de serpentín

Refrigerante recto
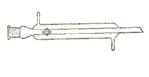
Es un refrigerante que también recibe el nombre de: Refrigerante de Liebing. Su nombre se debe a que su tubo interno es recto y al igual que los otros dos refrigerantes se utiliza como condensador.
Cristalizador

Matraz de reaccion
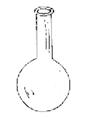
Es un recipiente que permite contener sustancias.
Matraz de destilación
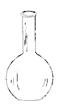
Balones
Balon sin base

Un balón de destilación es parte del llamado material de vidrio. Es un frasco de vidrio, de cuello largo y cuerpo esférico.
Balon con base
Leer más: http://www.monografias.com/trabajos72/instrumentos-laboratorio-quimica/instrumentos-laboratorio-quimica.shtml#ixzz3SuQCNQwZ
Suscribirse a:
Entradas (Atom)